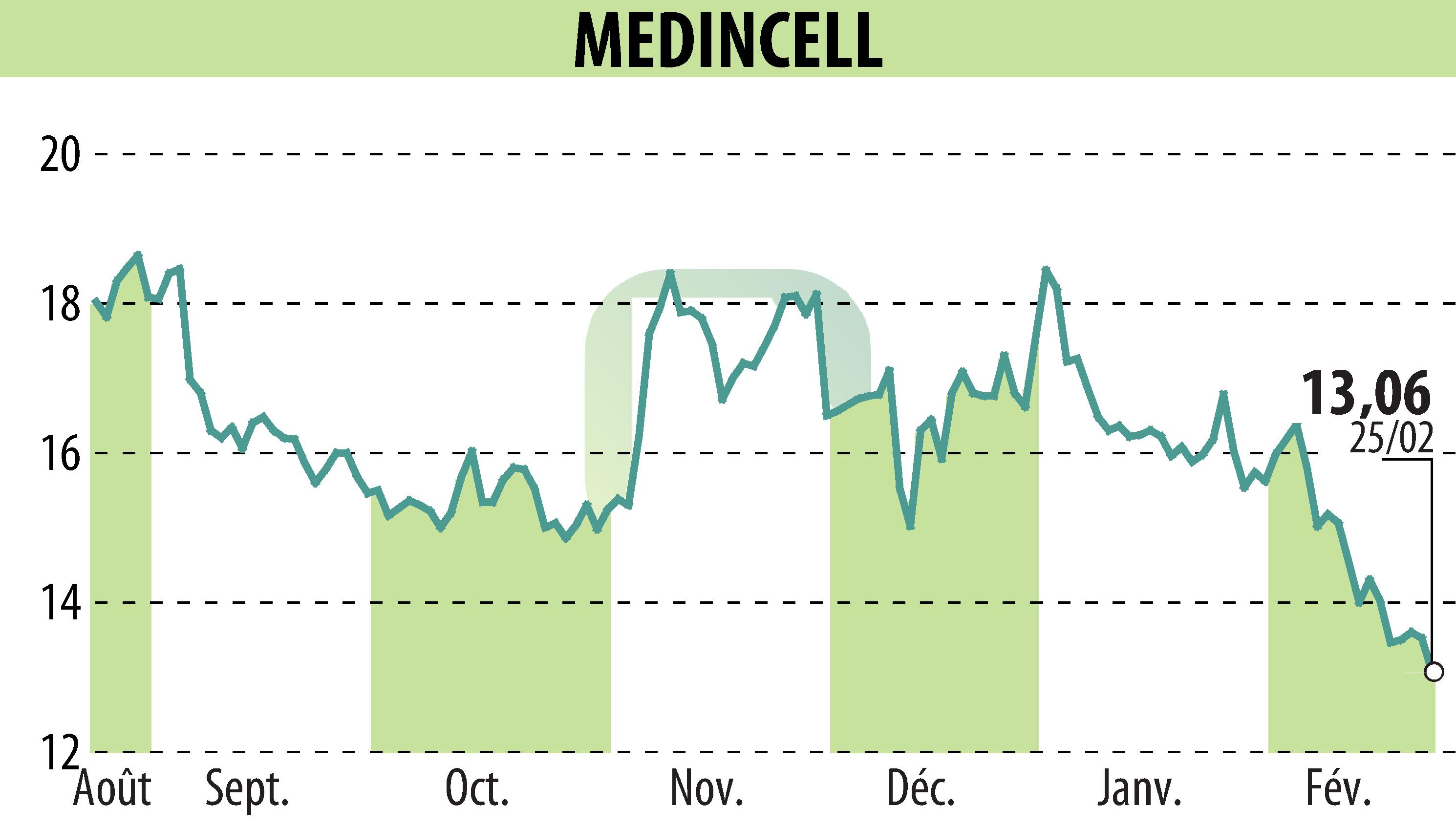
sur MEDINCELL (EPA:MEDCL)
La FDA accepte la demande d'utilisation d'UZEDY dans le traitement du trouble bipolaire I
Teva Pharmaceuticals et Medincell ont annoncé que la FDA avait accepté leur demande d'extension de l'indication d'UZEDY®, un antipsychotique injectable, pour inclure le traitement du trouble bipolaire de type I (TB-I). UZEDY est déjà approuvé aux États-Unis pour le traitement de la schizophrénie chez l'adulte par injection mensuelle ou bimensuelle.
La nouvelle demande s'appuie sur les données cliniques existantes de l'UZEDY et sur les conclusions de la FDA concernant les formulations de rispéridone précédemment approuvées pour le traitement de la BP-I. Cette acceptation souligne l'engagement de Teva à faire progresser les traitements en neurosciences.
La forme injectable à action prolongée d'UZEDY répond à des besoins non satisfaits dans le traitement de la BP-I, améliorant potentiellement l'observance du traitement par les patients. Teva supervisera les processus réglementaires et la commercialisation, Medincell étant éligible aux redevances sur les ventes nettes.
R. H.
Copyright © 2025 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de MEDINCELL
