sur Moderna, Inc. (NASDAQ:MRNA)
Moderna dépose une demande auprès de la FDA pour le vaccin JN.1 ciblant la COVID-19
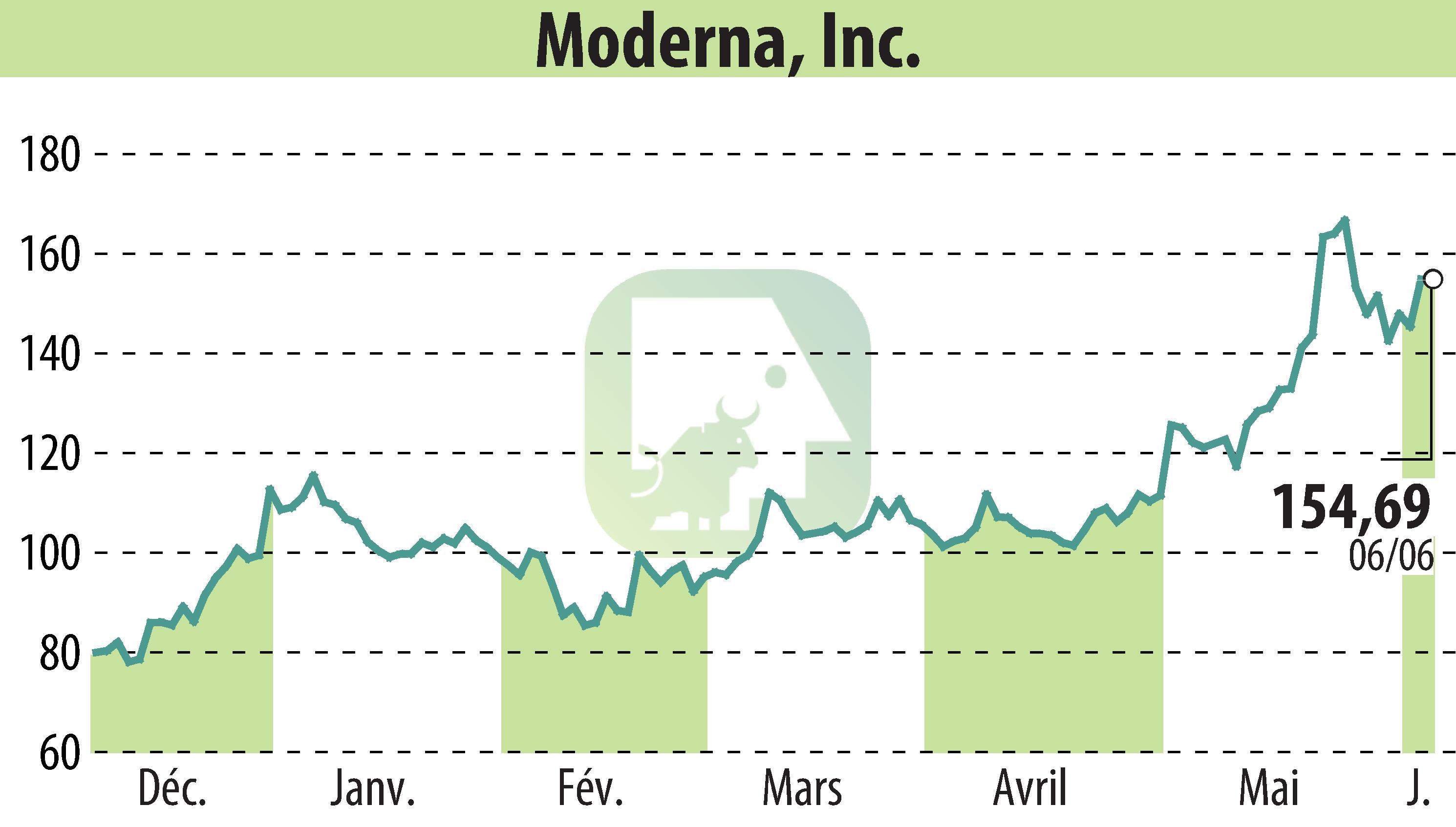
CAMBRIDGE, MA / ACCESSWIRE / 7 juin 2024 / Moderna, Inc. (NASDAQ : MRNA) a franchi une étape importante dans la lutte contre le COVID-19. La société a annoncé avoir soumis une demande à la Food and Drug Administration (FDA) des États-Unis pour sa formule Spikevax 2024-2025. Cette nouvelle version du vaccin cible la variante JN.1 du SRAS-CoV-2. La fabrication est en cours et les doses seront prêtes à être expédiées dès le mois d'août, en attendant l'approbation réglementaire.
La soumission suit les directives de la FDA selon lesquelles les vaccins COVID-19 pour la saison 2024-2025 devraient être mis à jour vers une composition monovalente JN.1. Cela correspond aux recommandations de l’Organisation mondiale de la santé (OMS) et de l’Agence européenne des médicaments (EMA). Les événements indésirables locaux les plus sollicités et signalés comprennent la douleur au site d'injection, tandis que les événements indésirables systémiques comprennent les maux de tête, la fatigue, la myalgie et les frissons.
Le PDG de Moderna, Stéphane Bancel, a souligné l'importance de se tenir au courant des vaccinations contre la COVID-19 pour se protéger contre les maladies respiratoires. La société soumet également des données aux régulateurs du monde entier pour faciliter l’enregistrement et la fourniture de sa formule Spikevax mise à jour à temps pour la prochaine saison de vaccination.
R. H.
Copyright © 2024 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de Moderna, Inc.
